Ditt meddelande har skickats.
Vi behandlar din begäran och återkommer till dig så snart som möjligt.
Formuläret har skickats in framgångsrikt.
Ytterligare information finns i din brevlåda.
AI håller på att förändra Läkemedelsindustrinoch ett av de mest betydelsefulla områdena är processen för läkemedelsutveckling. Med hjälp av avancerade maskininlärningsalgoritmer, t.ex. transformatormodeller och grafneurala nätverk, och stora datamängder påskyndar AI upptäckten av nya behandlingar och förbättrar effektiviteten i hela utvecklingsprocessen.
Innan vi kan utforma ett läkemedel måste vi identifiera det terapeutiska målet - ett specifikt enzym, en muterad gen eller en kritisk signalväg. Genom analys av storskaliga biologiska data, inklusive genomisk och transkriptomisk information från nästa generations sekvensering (NGS), hjälper AI till att identifiera de bästa terapeutiska möjligheterna, avslöja komplexa mönster och samband som traditionella metoder kan missa. Detta leder till upptäckten av nya målmolekyler och innovativa behandlingar.
AI optimerar preklinisk forskning genom att utnyttja data från in vitro- och in vivo-studier för att förutse substansers effekt och toxicitet. Denna metod hjälper forskarna att göra smarta val om vilka substanser de ska satsa på och därmed spara både tid och resurser. Dessutom kan AI optimera experimentell design i prekliniska urval av läkemedelskandidater för vidare utveckling.
AI förändrar läkemedelsdesignen genom att generera nya molekylära strukturer som är optimerade för effekt och säkerhet. AI-algoritmer identifierar lovande kandidater och utforskar den kemiska rymden bortom traditionella metoders begränsningar genom att analysera massiva datamängder av befintliga föreningar och deras målinteraktioner. Detta påskyndar upptäckten av innovativa behandlingar med potential att tillgodose medicinska behov som ännu inte tillgodosetts.
AI-driven prediktiv modellering och simulering förfinar läkemedelsdesignen ytterligare genom att efterlikna beteendet hos komplexa biologiska system. Denna in silico-metod förutser läkemedlets prestanda i olika stadier, från absorption och distribution till metabolism och utsöndring: på så sätt kan forskarna enkelt identifiera läkemedelskandidater med önskade egenskaper före kostsamma experimentella tester. Detta förbättrar avsevärt chanserna till klinisk framgång.
AI spelar en allt viktigare roll i kliniska prövningar. AI används för att analysera data från tidigare prövningar, identifiera mönster och förutse potentiella problem. Detta hjälper forskarna att utforma bättre prövningar, hitta rätt patienter och öka chanserna för ett lyckat resultat samtidigt som kostnaderna och tidsramarna minskar. AI kan också hjälpa dem att enkelt hitta och rekrytera patienter till kliniska prövningar. Den kan matcha patienter till prövningar baserat på deras specifika egenskaper och prövningskriterierna.

Utvecklingen av individanpassad medicin stöds av AI:s förmåga att analysera stora mängder av patienters genomdata och sjukdomshistoria för att identifiera individuella biomarkörer och utveckla riktade behandlingar. Dessutom analyserar AI verkliga bevis och övervakningsdata efter marknadsföring för att identifiera potentiella säkerhetsproblem och förbättra behandlingsresultaten i verkliga miljöer.

Innan vi kan utforma ett läkemedel måste vi identifiera det terapeutiska målet - ett specifikt enzym, en muterad gen eller en kritisk signalväg. Genom analys av storskaliga biologiska data, inklusive genomisk och transkriptomisk information från nästa generations sekvensering (NGS), hjälper AI till att identifiera de bästa terapeutiska möjligheterna, avslöja komplexa mönster och samband som traditionella metoder kan missa. Detta leder till upptäckten av nya målmolekyler och innovativa behandlingar.

AI optimerar preklinisk forskning genom att utnyttja data från in vitro- och in vivo-studier för att förutse substansers effekt och toxicitet. Denna metod hjälper forskarna att göra smarta val om vilka substanser de ska satsa på och därmed spara både tid och resurser. Dessutom kan AI optimera experimentell design i prekliniska urval av läkemedelskandidater för vidare utveckling.

AI förändrar läkemedelsdesignen genom att generera nya molekylära strukturer som är optimerade för effekt och säkerhet. AI-algoritmer identifierar lovande kandidater och utforskar den kemiska rymden bortom traditionella metoders begränsningar genom att analysera massiva datamängder av befintliga föreningar och deras målinteraktioner. Detta påskyndar upptäckten av innovativa behandlingar med potential att tillgodose medicinska behov som ännu inte tillgodosetts.

AI-driven prediktiv modellering och simulering förfinar läkemedelsdesignen ytterligare genom att efterlikna beteendet hos komplexa biologiska system. Denna in silico-metod förutser läkemedlets prestanda i olika stadier, från absorption och distribution till metabolism och utsöndring: på så sätt kan forskarna enkelt identifiera läkemedelskandidater med önskade egenskaper före kostsamma experimentella tester. Detta förbättrar avsevärt chanserna till klinisk framgång.

AI spelar en allt viktigare roll i kliniska prövningar. AI används för att analysera data från tidigare prövningar, identifiera mönster och förutse potentiella problem. Detta hjälper forskarna att utforma bättre prövningar, hitta rätt patienter och öka chanserna för ett lyckat resultat samtidigt som kostnaderna och tidsramarna minskar. AI kan också hjälpa dem att enkelt hitta och rekrytera patienter till kliniska prövningar. Den kan matcha patienter till prövningar baserat på deras specifika egenskaper och prövningskriterierna.

Utvecklingen av individanpassad medicin stöds av AI:s förmåga att analysera stora mängder av patienters genomdata och sjukdomshistoria för att identifiera individuella biomarkörer och utveckla riktade behandlingar. Dessutom analyserar AI verkliga bevis och övervakningsdata efter marknadsföring för att identifiera potentiella säkerhetsproblem och förbättra behandlingsresultaten i verkliga miljöer.

Multiomisk dataanalys
Analys av kliniska data
Analys av vetenskapliga forskningsdata
De novo läkemedelsdesign
ML + molekylär dynamik
ML + molekylär dockning
ML + farmakokinetisk modellering
Identifiering av träff
Stratifiering av patienter
Datautvinning
Optimering av läkemedel

Förbättra din AI-drivna läkemedelsupptäckt med Innowise.
AI innebär en total förändring för läkemedelsindustrin: den erbjuder många fördelar som gör processen för upptäckt och utveckling av läkemedel smidigare och effektivare.
Tack vare den snabba analysen av stora datamängder kan ML-algoritmer påskynda varje steg, från identifiering av mål och optimering av ledtrådar till utformning av kliniska prövningar och omplacering av läkemedel. Jämfört med traditionella metoder förkortar denna snabbare takt avsevärt utvecklingstiderna och minskar kostnaderna.

Korrekt tränade AI-modeller kan förutsäga kritiska egenskaper som målbindningsaffinitet, farmakokinetiska/farmakodynamiska profiler och ADMET-egenskaper - och därmed hjälpa forskare att utforma läkemedel med förbättrad effekt. Detta AI-drivna tillvägagångssätt optimerar läkemedelskandidater för förbättrad måluppfyllelse, minskad toxicitet och i slutändan bättre patientresultat.

AI-modeller hjälper också till att optimera utformningen av kliniska prövningar genom att identifiera idealiska patientkohorter med hjälp av prediktiva biomarkörer och förfina prövningsprotokollen för ökad effektivitet. Detta riktade tillvägagångssätt ökar sannolikheten för framgångsrika prövningsresultat och påskyndar leveransen av livsförändrande läkemedel till patienterna.

AI ökar avsevärt förutsägbarheten i läkemedelsutvecklingen och hjälper forskarna att förutse läkemedlens beteende, effekt och säkerhetsprofil. Med hjälp av en rad olika tekniker identifierar AI tidigt lovande kandidater och potentiella skulder och påskyndar utvecklingstiderna.

AI-algoritmer analyserar stora datamängder för att identifiera nya terapeutiska tillämpningar för befintliga läkemedel. Denna strategi för att återanvända läkemedel påskyndar utvecklingstiden eftersom dessa läkemedel redan har etablerade säkerhetsprofiler och kliniska data, vilket minskar behovet av omfattande och kostsamma de novo-prövningar.

AI analyserar patientspecifika data, inklusive genetiska och molekylära profiler, för att skräddarsy behandlingar för optimal effekt. AI kan till exempel förutsäga en individs svar på en specifik cellgiftsbehandling baserat på tumörens genetiska sammansättning, så att onkologer kan välja den mest effektiva behandlingen och samtidigt minimera biverkningarna. Detta individanpassade tillvägagångssätt maximerar nyttan för den enskilda patienten.
AI automatiserar högkapacitetsscreening av stora substansbibliotek för att identifiera lovande läkemedelskandidater med större effektivitet än traditionella metoder. Genom att analysera molekylstrukturer och förutsäga deras interaktioner med målproteiner kan AI prioritera föreningar med störst sannolikhet att lyckas, vilket avsevärt minskar den tid och de kostnader som är förknippade med tidiga stadier av läkemedelsupptäckt.
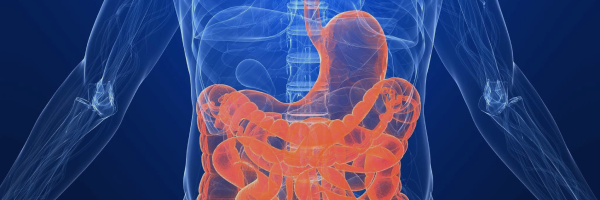
AI-algoritmer analyserar samspelet mellan ingredienser och deras inverkan på stabilitet, löslighet och biotillgänglighet och förutspår optimala läkemedelsformuleringar. AI kan t.ex. modellera hur olika hjälpämnen påverkar ett läkemedels upplösningshastighet och absorption i mag-tarmkanalen, vilket leder till förbättrad läkemedelseffekt, enklare administrering (t.ex. oral i stället för intravenös) och bättre patientföljsamhet.
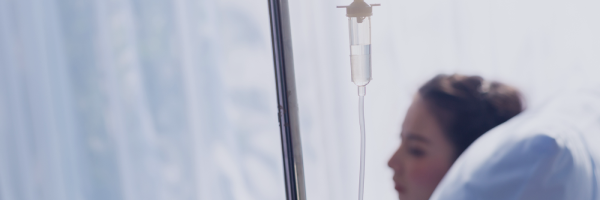
AI-driven analys identifierar idealiska kandidater för kliniska prövningar baserat på en omfattande analys av patientdata, inklusive sjukdomshistoria, demografi och genetisk information. Den identifierar de patienter som har störst sannolikhet att svara positivt på en behandling. Denna riktade rekryteringsstrategi förbättrar effektiviteten i prövningarna, ökar framgångsgraden och påskyndar i slutändan leveransen av nya behandlingar till patienterna.

Tack vare den snabba analysen av stora datamängder kan ML-algoritmer påskynda varje steg, från identifiering av mål och optimering av ledtrådar till utformning av kliniska prövningar och omplacering av läkemedel. Jämfört med traditionella metoder förkortar denna snabbare takt avsevärt utvecklingstiderna och minskar kostnaderna.

Korrekt tränade AI-modeller kan förutsäga kritiska egenskaper som målbindningsaffinitet, farmakokinetiska/farmakodynamiska profiler och ADMET-egenskaper - och därmed hjälpa forskare att utforma läkemedel med förbättrad effekt. Detta AI-drivna tillvägagångssätt optimerar läkemedelskandidater för förbättrad måluppfyllelse, minskad toxicitet och i slutändan bättre patientresultat.

AI-modeller hjälper också till att optimera utformningen av kliniska prövningar genom att identifiera idealiska patientkohorter med hjälp av prediktiva biomarkörer och förfina prövningsprotokollen för ökad effektivitet. Detta riktade tillvägagångssätt ökar sannolikheten för framgångsrika prövningsresultat och påskyndar leveransen av livsförändrande läkemedel till patienterna.

AI ökar avsevärt förutsägbarheten i läkemedelsutvecklingen och hjälper forskarna att förutse läkemedlens beteende, effekt och säkerhetsprofil. Med hjälp av en rad olika tekniker identifierar AI tidigt lovande kandidater och potentiella skulder och påskyndar utvecklingstiderna.

AI-algoritmer analyserar stora datamängder för att identifiera nya terapeutiska tillämpningar för befintliga läkemedel. Denna strategi för att återanvända läkemedel påskyndar utvecklingstiden eftersom dessa läkemedel redan har etablerade säkerhetsprofiler och kliniska data, vilket minskar behovet av omfattande och kostsamma de novo-prövningar.

AI analyserar patientspecifika data, inklusive genetiska och molekylära profiler, för att skräddarsy behandlingar för optimal effekt. AI kan till exempel förutsäga en individs svar på en specifik cellgiftsbehandling baserat på tumörens genetiska sammansättning, så att onkologer kan välja den mest effektiva behandlingen och samtidigt minimera biverkningarna. Detta individanpassade tillvägagångssätt maximerar nyttan för den enskilda patienten.

AI automatiserar högkapacitetsscreening av stora substansbibliotek för att identifiera lovande läkemedelskandidater med större effektivitet än traditionella metoder. Genom att analysera molekylstrukturer och förutsäga deras interaktioner med målproteiner kan AI prioritera föreningar med störst sannolikhet att lyckas, vilket avsevärt minskar den tid och de kostnader som är förknippade med tidiga stadier av läkemedelsupptäckt.

AI-algoritmer analyserar samspelet mellan ingredienser och deras inverkan på stabilitet, löslighet och biotillgänglighet och förutspår optimala läkemedelsformuleringar. AI kan t.ex. modellera hur olika hjälpämnen påverkar ett läkemedels upplösningshastighet och absorption i mag-tarmkanalen, vilket leder till förbättrad läkemedelseffekt, enklare administrering (t.ex. oral i stället för intravenös) och bättre patientföljsamhet.

AI-driven analys identifierar idealiska kandidater för kliniska prövningar baserat på en omfattande analys av patientdata, inklusive sjukdomshistoria, demografi och genetisk information. Den identifierar de patienter som har störst sannolikhet att svara positivt på en behandling. Denna riktade rekryteringsstrategi förbättrar effektiviteten i prövningarna, ökar framgångsgraden och påskyndar i slutändan leveransen av nya behandlingar till patienterna.


Vi utvecklade en maskininlärningsmodell för att förutsäga vattenlöslighet för nya småmolekylära hämmare riktade mot protein X. Med hjälp av experimentellt bestämda löslighetsdata tränade vi en anpassad ML-pipeline som utnyttjar molekylära deskriptorer. Modellen uppnådde en R-kvadrat på 0,70 vid extern validering, vilket gör den till ett värdefullt verktyg för screening av virtuella bibliotek och prioritering av föreningar för syntes.
Vi utvecklade en maskininlärningsmodell för att förutsäga vattenlöslighet för nya småmolekylära hämmare riktade mot protein X. Med hjälp av experimentellt bestämda löslighetsdata tränade vi en anpassad ML-pipeline som utnyttjar molekylära deskriptorer. Modellen uppnådde en R-kvadrat på 0,70 vid extern validering, vilket gör den till ett värdefullt verktyg för screening av virtuella bibliotek och prioritering av föreningar för syntes.
Under utvecklingsarbetet gav femfaldig korsvalidering ett genomsnittligt R-kvadrat på 0,75. Även om modellen inte ersätter experimentella mätningar bidrar den till att påskynda optimeringsprocessen genom att möjliggöra snabb virtuell screening av substansbibliotek före syntes och testning.

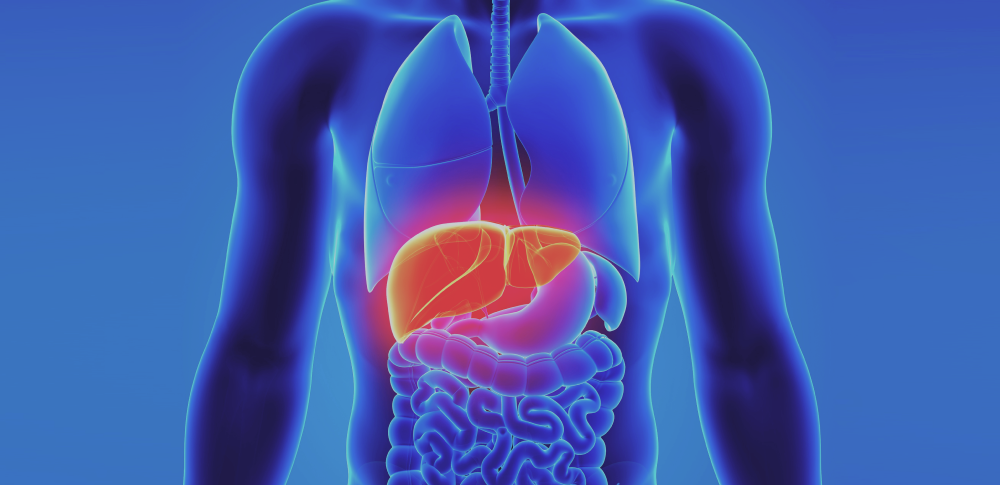
Vi förbättrade förutsägelserna av leverclearance i en GastroPlus PBPK-modell med hjälp av en hybrid maskininlärningsmetod. Genom att kombinera LightGBM och D-MPNN grafneurala nätverk uppnådde vår modell en R-kvadrat på 0,82 i korsvalidering. Integrationen minskade det genomsnittliga vikfelet från 2,5 till 2,0 jämfört med traditionella in vitro-skaleringsmetoder, vilket möjliggör mer tillförlitliga förutsägelser av läkemedelsexponering.
Vi förbättrade förutsägelserna av leverclearance i en GastroPlus PBPK-modell med hjälp av en hybrid maskininlärningsmetod. Genom att kombinera LightGBM och D-MPNN grafneurala nätverk uppnådde vår modell en R-kvadrat på 0,82 i korsvalidering. Integrationen minskade det genomsnittliga vikfelet från 2,5 till 2,0 jämfört med traditionella in vitro-skaleringsmetoder, vilket möjliggör mer tillförlitliga förutsägelser av läkemedelsexponering.
Studien använde 150 föreningars kemiska strukturer och stabilitetsdata för hepatocyter in vitro. Vi utvecklade en anpassad pipeline med Gradient Boosting Machine-modell med LightGBM och Directed Message Passing Neural Network-arkitektur. Den förbättrade noggrannheten gav direkt stöd för ett mer välinformerat dosval för prekliniska studier.
Innan vi kan utforma ett läkemedel måste vi identifiera det terapeutiska målet - oavsett om det är ett specifikt enzym, en muterad gen eller en kritisk signalväg. Genom analys av storskaliga biologiska data, inklusive genomisk och transkriptomisk information från nästa generations sekvensering (NGS), hjälper AI till att identifiera de bästa möjligheterna för terapeutisk inriktning. Avancerade maskininlärningsalgoritmer, t.ex. grafneurala nätverk och transfer learning.
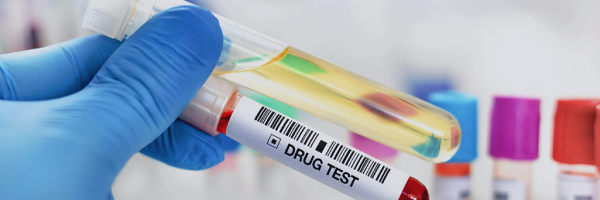
Vi skapade ett Twitter-övervakningssystem för att upptäcka biverkningar (ADR) för läkemedlet Y. Med hjälp av NLP och en anpassad klassificerare för maskininlärning uppnådde vi en F1-score på 0,78 på 5.000 annoterade tweets. Systemet identifierade framgångsrikt flera potentiella signaler om läkemedelssäkerhet under en 3-månadersperiod och fungerade som ett tidigt varningssystem som komplement till traditionell säkerhetsövervakning av läkemedel.
Systemet använde named entity recognition och sentimentanalys för att filtrera relevanta tweets. Vår klassificerare var särskilt tränad för att skilja mellan äkta ADR-omnämnanden och allmänna läkemedelsdiskussioner. Identifierade signaler vidarebefordrades till farmakovigilansteamet för vidare utredning och bearbetning, vilket förbättrar de traditionella metoderna för säkerhetsövervakning.


Dela:













Ditt meddelande har skickats.
Vi behandlar din begäran och återkommer till dig så snart som möjligt.

Genom att registrera dig godkänner du vår Integritetspolicy, inklusive användning av cookies och överföring av din personliga information.